Pneumonia nosokomial adalah infeksi nosokomial yang paling umum dan serius, dengan pneumonia terkait ventilator (VAP) mencapai 40%. VAP yang disebabkan oleh patogen refrakter masih menjadi masalah klinis yang sulit. Selama bertahun-tahun, pedoman telah merekomendasikan berbagai intervensi (seperti sedasi terarah dan elevasi kepala) untuk mencegah VAP, tetapi VAP terjadi pada hingga 40% pasien dengan intubasi trakea, yang mengakibatkan rawat inap yang lebih lama, peningkatan penggunaan antibiotik, dan kematian. Orang-orang selalu mencari tindakan pencegahan yang lebih efektif.
Pneumonia terkait ventilator (VAP) adalah pneumonia baru yang berkembang 48 jam setelah intubasi trakea dan merupakan infeksi nosokomial yang paling umum dan mematikan di unit perawatan intensif (ICU). Pedoman American Society of Infectious Diseases (AID) tahun 2016 telah membedakan VAP dari definisi pneumonia yang didapat di rumah sakit (HAP) (HAP hanya merujuk pada pneumonia yang terjadi setelah rawat inap tanpa selang trakea dan tidak terkait dengan ventilasi mekanis; VAP adalah pneumonia setelah intubasi trakea dan ventilasi mekanis), dan European Society serta Tiongkok meyakini bahwa VAP masih merupakan jenis HAP yang khusus [1-3].
Pada pasien yang menerima ventilasi mekanis, insidensi VAP berkisar antara 9% hingga 27%, tingkat mortalitas diperkirakan sebesar 13%, dan dapat menyebabkan peningkatan penggunaan antibiotik sistemik, ventilasi mekanis yang lebih lama, lama tinggal di ICU, dan peningkatan biaya [4-6]. HAP/VAP pada pasien non-imunodefisiensi biasanya disebabkan oleh infeksi bakteri, dan distribusi patogen umum dan karakteristik resistensinya bervariasi menurut wilayah, kelas rumah sakit, populasi pasien, dan paparan antibiotik, dan berubah seiring waktu. Pseudomonas aeruginosa mendominasi patogen terkait VAP di Eropa dan Amerika, sementara lebih banyak Acinetobacter baumannii diisolasi di rumah sakit tersier di Cina. Sepertiga hingga setengah dari semua kematian terkait VAP secara langsung disebabkan oleh infeksi, dengan tingkat mortalitas kasus yang disebabkan oleh Pseudomonas aeruginosa dan acinetobacter lebih tinggi [7,8].
Karena heterogenitas VAP yang kuat, spesifisitas diagnostik manifestasi klinis, pencitraan dan tes laboratoriumnya rendah, dan rentang diagnosis bandingnya luas, yang membuatnya sulit untuk mendiagnosis VAP pada waktunya. Pada saat yang sama, resistensi bakteri menimbulkan tantangan serius bagi pengobatan VAP. Diperkirakan bahwa risiko mengembangkan VAP adalah 3%/hari selama 5 hari pertama penggunaan ventilasi mekanis, 2%/hari antara 5 dan 10 hari, dan 1%/hari untuk sisa waktu. Insidensi puncak umumnya terjadi setelah 7 hari ventilasi, jadi ada jendela di mana infeksi dapat dicegah sejak dini [9,10]. Banyak penelitian telah melihat pencegahan VAP, tetapi meskipun ada penelitian dan upaya selama beberapa dekade untuk mencegah VAP (seperti menghindari intubasi, mencegah intubasi ulang, mengurangi sedasi, meninggikan kepala tempat tidur sebesar 30° hingga 45°, dan perawatan mulut), insidensi tampaknya tidak menurun dan beban medis terkait tetap sangat tinggi.
Antibiotik inhalasi telah digunakan untuk mengobati infeksi saluran napas kronis sejak tahun 1940-an. Karena dapat memaksimalkan pengiriman obat ke lokasi target infeksi (yaitu saluran napas) dan mengurangi efek samping sistemik, ia telah menunjukkan nilai aplikasi yang baik dalam berbagai penyakit. Antibiotik inhalasi sekarang disetujui oleh Badan Pengawas Obat dan Makanan AS (FDA) dan Badan Obat-obatan Eropa (EMA) untuk digunakan dalam fibrosis kistik. Antibiotik inhalasi dapat secara signifikan mengurangi jumlah bakteri dan frekuensi eksaserbasi pada bronkiektasis tanpa meningkatkan efek samping secara keseluruhan, dan pedoman saat ini telah mengakuinya sebagai pengobatan lini pertama untuk pasien dengan infeksi pseudomonas aeruginosa dan eksaserbasi yang sering; Antibiotik inhalasi selama periode perioperatif transplantasi paru-paru juga dapat digunakan sebagai obat adjuvan atau profilaksis [11,12]. Namun dalam pedoman VAP AS 2016, para ahli kurang percaya diri dalam efektivitas antibiotik inhalasi adjuvan karena kurangnya uji coba terkontrol acak yang besar. Uji coba Fase 3 (INHALE) yang diterbitkan pada tahun 2020 juga gagal memperoleh hasil positif (menghirup antibiotik intravena yang dibantu amikasin untuk infeksi bakteri Gram-negatif yang disebabkan oleh pasien VAP, uji coba efikasi fase 3 yang bersifat double-blind, acak, terkontrol plasebo, total 807 pasien, pengobatan sistemik + inhalasi amikasin yang dibantu selama 10 hari).
Dalam konteks ini, tim yang dipimpin oleh para peneliti dari Pusat Rumah Sakit Universitas Regional Tours (CHRU) di Prancis mengadopsi strategi penelitian yang berbeda dan melakukan uji coba efikasi terkontrol acak, multisenter, tersamar ganda, dan diinisiasi oleh peneliti (AMIKINHAL). Amikasin inhalasi atau plasebo untuk pencegahan VAP dibandingkan dalam 19 kasus di Prancis [13].
Sebanyak 847 pasien dewasa dengan ventilasi mekanis invasif antara 72 dan 96 jam secara acak dibagi menjadi dua kelompok: 1 ...
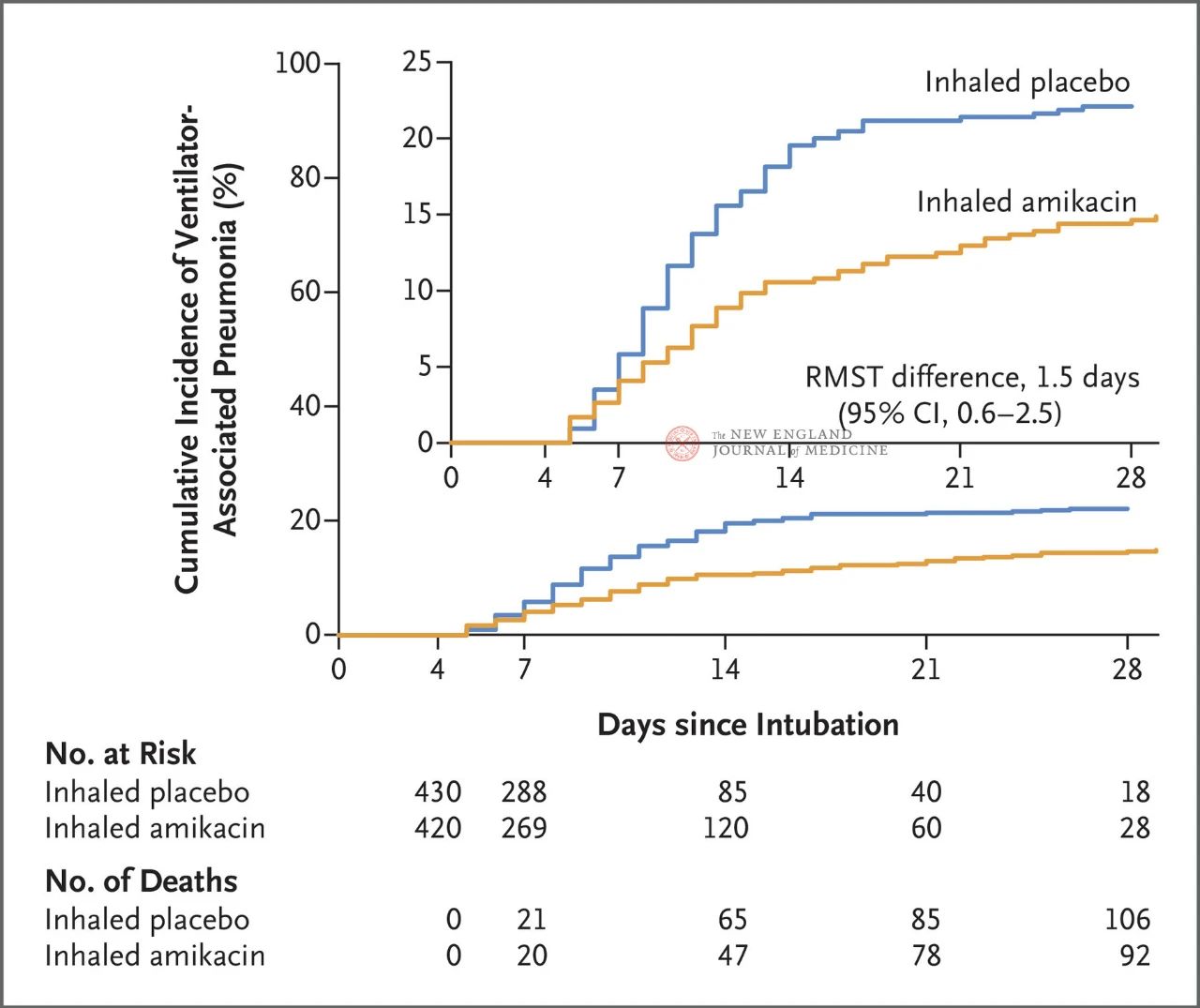
Hasil uji coba menunjukkan bahwa pada hari ke-28, 62 pasien (15%) dalam kelompok amikasin telah mengembangkan VAP dan 95 pasien (22%) dalam kelompok plasebo telah mengembangkan VAP (perbedaan kelangsungan hidup rata-rata terbatas untuk VAP adalah 1,5 hari; 95% CI, 0,6~2,5; P=0,004).
Dari segi keamanan, tujuh pasien (1,7%) pada kelompok amikasin dan empat pasien (0,9%) pada kelompok plasebo mengalami efek samping serius terkait uji klinis. Di antara mereka yang tidak mengalami cedera ginjal akut saat pengacakan, 11 pasien (4%) pada kelompok amikasin dan 24 pasien (8%) pada kelompok plasebo mengalami cedera ginjal akut pada hari ke-28 (HR, 0,47; 95% CI, 0,23~0,96).
Uji klinis ini memiliki tiga poin penting. Pertama, dalam hal desain studi, uji coba AMIKINHAL mengacu pada uji coba IASIS (uji coba fase 2 paralel, acak, tersamar ganda, terkontrol plasebo, yang melibatkan 143 pasien). Uji coba ini bertujuan untuk mengevaluasi keamanan dan efektivitas pengobatan sistemik inhalasi amikasin-fosfomisin untuk infeksi bakteri gram negatif yang disebabkan oleh VAP dan uji coba INHALE yang berakhir dengan hasil negatif. Pelajaran yang dipetik, yang berfokus pada pencegahan VAP, telah menghasilkan hasil yang relatif baik. Mengingat karakteristik mortalitas yang tinggi dan lama rawat inap di rumah sakit pada pasien dengan ventilasi mekanis dan VAP, jika inhalasi amikasin dapat mencapai hasil yang berbeda secara signifikan dalam mengurangi mortalitas dan lama rawat inap pada pasien ini, hal ini akan lebih bermanfaat bagi praktik klinis. Namun, mengingat heterogenitas pengobatan dan perawatan yang terlambat pada setiap pasien dan setiap pusat, terdapat sejumlah faktor perancu yang dapat mengganggu studi ini, sehingga mungkin sulit untuk mendapatkan hasil positif yang disebabkan oleh antibiotik inhalasi. Oleh karena itu, studi klinis yang berhasil tidak hanya memerlukan desain studi yang baik, tetapi juga pemilihan titik akhir primer yang tepat.
Kedua, meskipun antibiotik aminoglikosida tidak direkomendasikan sebagai obat tunggal dalam berbagai pedoman VAP, antibiotik aminoglikosida dapat mencakup patogen umum pada pasien VAP (termasuk pseudomonas aeruginosa, acinetobacter, dll.), dan karena penyerapannya yang terbatas pada sel epitel paru-paru, konsentrasi tinggi di tempat infeksi, dan toksisitas sistemik yang rendah. Antibiotik aminoglikosida secara luas lebih disukai di antara antibiotik inhalasi. Makalah ini konsisten dengan perkiraan komprehensif ukuran efek pemberian gentamisin intratrakeal dalam sampel kecil yang dipublikasikan sebelumnya, yang secara bersama-sama menunjukkan efek antibiotik aminoglikosida inhalasi dalam mencegah VAP. Perlu juga dicatat bahwa sebagian besar kontrol plasebo yang dipilih dalam uji coba terkait antibiotik inhalasi adalah salin normal. Namun, mengingat bahwa inhalasi salin normal yang diatomisasi sendiri dapat memainkan peran tertentu dalam mengencerkan sputum dan membantu ekspektoran, salin normal dapat menyebabkan gangguan tertentu dalam analisis hasil studi, yang harus dipertimbangkan secara komprehensif dalam studi ini.
Lebih lanjut, adaptasi lokal pengobatan HAP/VAP penting, seperti halnya profilaksis antibiotik. Pada saat yang sama, terlepas dari lamanya waktu intubasi, ekologi ICU lokal merupakan faktor risiko terpenting untuk infeksi dengan bakteri yang resistan terhadap banyak obat. Oleh karena itu, perawatan empiris harus merujuk pada data mikrobiologi rumah sakit setempat sebanyak mungkin, dan tidak dapat secara membabi buta merujuk pada pedoman atau pengalaman rumah sakit tersier. Pada saat yang sama, pasien sakit kritis yang membutuhkan ventilasi mekanis sering dikombinasikan dengan penyakit multi-sistem, dan di bawah tindakan gabungan dari beberapa faktor seperti keadaan stres, mungkin juga ada fenomena mikroba usus yang berinteraksi dengan paru-paru. Heterogenitas tinggi penyakit yang disebabkan oleh superposisi internal dan eksternal juga menentukan bahwa promosi klinis skala besar dari setiap intervensi baru masih jauh.
Waktu posting: 02-Des-2023