Penghargaan Penelitian Medis Dasar Lasker tahun ini diberikan kepada Demis Hassabis dan John Jumper atas kontribusi mereka dalam penciptaan sistem kecerdasan buatan AlphaFold yang memprediksi struktur tiga dimensi protein berdasarkan urutan asam amino tingkat pertama.
Hasil mereka memecahkan masalah yang telah lama mengganggu komunitas ilmiah dan membuka pintu bagi percepatan penelitian di seluruh bidang biomedis. Protein memainkan peran penting dalam perkembangan penyakit: pada penyakit Alzheimer, protein melipat dan menggumpal; pada kanker, fungsi regulasinya hilang; pada gangguan metabolisme bawaan, protein tidak berfungsi; pada fibrosis kistik, protein masuk ke ruang yang salah di dalam sel. Ini hanyalah beberapa dari sekian banyak mekanisme penyebab penyakit. Model struktur protein yang terperinci dapat memberikan konfigurasi atom, mendorong desain atau pemilihan molekul berafinitas tinggi, dan mempercepat penemuan obat.
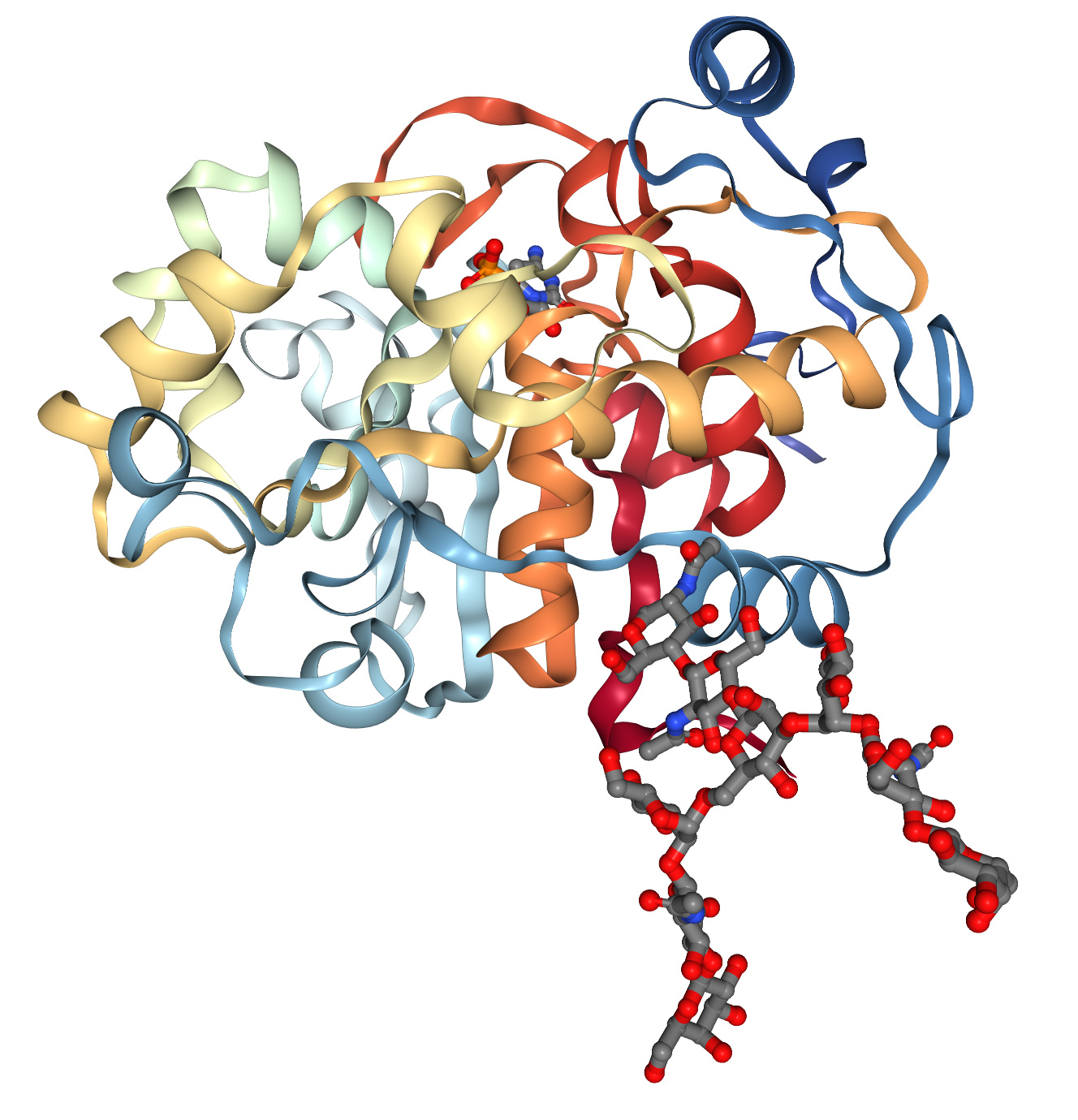
Struktur protein umumnya ditentukan oleh kristalografi sinar-X, resonansi magnetik nuklir dan mikroskopi krio-elektron. Metode-metode ini mahal dan memakan waktu. Hal ini menghasilkan database struktur protein 3D yang ada dengan hanya sekitar 200.000 data struktural, sementara teknologi sekuensing DNA telah menghasilkan lebih dari 8 juta sekuens protein. Pada tahun 1960-an, Anfinsen dkk. menemukan bahwa sekuens 1D asam amino dapat secara spontan dan berulang melipat menjadi konformasi tiga dimensi fungsional (Gambar 1A), dan bahwa "chaperone" molekuler dapat mempercepat dan memfasilitasi proses ini. Pengamatan ini mengarah pada tantangan 60 tahun dalam biologi molekuler: memprediksi struktur 3D protein dari sekuens 1D asam amino. Dengan keberhasilan Proyek Genom Manusia, kemampuan kita untuk mendapatkan sekuens asam amino 1D telah sangat meningkat, dan tantangan ini menjadi lebih mendesak.
Memprediksi struktur protein sulit karena beberapa alasan. Pertama, semua kemungkinan posisi tiga dimensi setiap atom dalam setiap asam amino membutuhkan banyak eksplorasi. Kedua, protein memanfaatkan komplementaritas secara maksimal dalam struktur kimianya untuk mengonfigurasi atom secara efisien. Karena protein biasanya memiliki ratusan "donor" ikatan hidrogen (biasanya oksigen) yang seharusnya dekat dengan "akseptor" ikatan hidrogen (biasanya nitrogen yang terikat pada hidrogen), akan sangat sulit untuk menemukan konformasi di mana hampir setiap donor dekat dengan akseptor. Ketiga, contoh untuk pelatihan metode eksperimen terbatas, sehingga perlu untuk memahami potensi interaksi tiga dimensi antar asam amino berdasarkan sekuens 1D menggunakan informasi tentang evolusi protein yang relevan.
Fisika pertama kali digunakan untuk memodelkan interaksi atom dalam pencarian konformasi terbaik, dan sebuah metode dikembangkan untuk memprediksi struktur protein. Karplus, Levitt, dan Warshel dianugerahi Hadiah Nobel Kimia 2013 atas karya mereka dalam simulasi komputasional protein. Namun, metode berbasis fisika membutuhkan komputasi yang mahal dan memerlukan pemrosesan perkiraan, sehingga struktur tiga dimensi yang presisi tidak dapat diprediksi. Pendekatan "berbasis pengetahuan" lainnya adalah menggunakan basis data struktur dan sekuens yang diketahui untuk melatih model melalui kecerdasan buatan dan pembelajaran mesin (AI-ML). Hassabis dan Jumper menerapkan elemen fisika dan AI-ML, tetapi inovasi dan peningkatan kinerja pendekatan ini terutama berasal dari AI-ML. Kedua peneliti ini secara kreatif menggabungkan basis data publik yang besar dengan sumber daya komputasi kelas industri untuk menciptakan AlphaFold.
Bagaimana kita tahu mereka telah "memecahkan" teka-teki prediksi struktural? Pada tahun 1994, kompetisi Critical Assessment of Structure Prediction (CASP) didirikan, yang bertemu setiap dua tahun untuk melacak kemajuan prediksi struktural. Para peneliti akan berbagi urutan 1D dari protein yang strukturnya baru-baru ini mereka pecahkan, tetapi hasilnya belum dipublikasikan. Prediktor memprediksi struktur tiga dimensi menggunakan urutan 1D ini, dan evaluator secara independen menilai kualitas hasil prediksi dengan membandingkannya dengan struktur tiga dimensi yang disediakan oleh eksperimentalis (disediakan hanya untuk evaluator). CASP melakukan tinjauan buta sejati dan mencatat lompatan kinerja berkala yang terkait dengan inovasi metodologis. Pada Konferensi CASP ke-14 pada tahun 2020, hasil prediksi AlphaFold menunjukkan lompatan kinerja yang sedemikian rupa sehingga penyelenggara mengumumkan bahwa masalah prediksi struktur 3D telah terpecahkan: akurasi sebagian besar prediksi mendekati akurasi pengukuran eksperimental.
Makna yang lebih luas adalah bahwa karya Hassabis dan Jumper secara meyakinkan menunjukkan bagaimana AI-ML dapat mentransformasi sains. Penelitian mereka menunjukkan bahwa AI-ML dapat membangun hipotesis ilmiah yang kompleks dari berbagai sumber data, bahwa mekanisme atensi (mirip dengan yang ada di ChatGPT) dapat menemukan dependensi dan korelasi kunci dalam sumber data, dan bahwa AI-ML dapat menilai sendiri kualitas hasil keluarannya. AI-ML pada dasarnya adalah melakukan sains.
Waktu posting: 23 Sep 2023