Kaheksia adalah penyakit sistemik yang ditandai dengan penurunan berat badan, atrofi otot dan jaringan adiposa, serta peradangan sistemik. Kaheksia merupakan salah satu komplikasi utama dan penyebab kematian pada pasien kanker. Diperkirakan insidensi kaheksia pada pasien kanker dapat mencapai 25% hingga 70%, dan sekitar 9 juta orang di seluruh dunia menderita kaheksia setiap tahun, 80% di antaranya diperkirakan meninggal dalam satu tahun setelah diagnosis. Selain itu, kaheksia secara signifikan memengaruhi kualitas hidup (QOL) pasien dan memperburuk toksisitas terkait pengobatan.
Intervensi kaheksia yang efektif sangat penting untuk meningkatkan kualitas hidup dan prognosis pasien kanker. Namun, meskipun terdapat beberapa kemajuan dalam studi mekanisme patofisiologis kaheksia, banyak obat yang dikembangkan berdasarkan mekanisme yang memungkinkan hanya sebagian efektif atau bahkan tidak efektif. Saat ini belum ada pengobatan efektif yang disetujui oleh Badan Pengawas Obat dan Makanan AS (FDA).
Kaheksia (sindrom penyusutan) sangat umum terjadi pada pasien dengan berbagai jenis kanker, yang seringkali mengakibatkan penurunan berat badan, penyusutan otot, penurunan kualitas hidup, gangguan fungsi, dan pemendekan kelangsungan hidup. Menurut standar internasional yang disepakati, sindrom multifaktorial ini didefinisikan sebagai indeks massa tubuh (IMT, berat badan [kg] dibagi tinggi badan [m] kuadrat) kurang dari 20 atau, pada pasien dengan sarkopenia, penurunan berat badan lebih dari 5% dalam enam bulan, atau penurunan berat badan lebih dari 2%. Saat ini, belum ada obat yang disetujui di Amerika Serikat dan Eropa secara khusus untuk pengobatan kaheksia kanker, sehingga pilihan pengobatannya terbatas.
Pedoman terbaru yang merekomendasikan olanzapine dosis rendah untuk meningkatkan nafsu makan dan berat badan pada pasien kanker stadium lanjut sebagian besar didasarkan pada hasil studi satu pusat. Selain itu, penggunaan analog progesteron atau glukokortikoid jangka pendek mungkin memberikan manfaat terbatas, tetapi terdapat risiko efek samping yang merugikan (seperti penggunaan progesteron yang berhubungan dengan kejadian tromboemboli). Uji klinis obat lain belum menunjukkan efikasi yang memadai untuk mendapatkan persetujuan regulatori. Meskipun anamorine (versi oral dari peptida pelepas hormon pertumbuhan) telah disetujui di Jepang untuk pengobatan kaheksia kanker, obat tersebut hanya meningkatkan komposisi tubuh sampai batas tertentu, tidak meningkatkan kekuatan genggaman, dan pada akhirnya tidak disetujui oleh Badan Pengawas Obat dan Makanan AS (FDA). Terdapat kebutuhan mendesak akan pengobatan yang aman, efektif, dan tepat sasaran untuk kaheksia kanker.
Faktor diferensiasi pertumbuhan 15 (GDF-15) adalah sitokin yang diinduksi stres yang berikatan dengan protein alfa-like reseptor keluarga faktor neurotropik turunan glia (GFRAL) di otak posterior. Jalur GDF-15-GFRAL telah diidentifikasi sebagai regulator utama anoreksia dan pengaturan berat badan, serta berperan dalam patogenesis kaheksia. Pada model hewan, GDF-15 dapat menginduksi kaheksia, dan penghambatan GDF-15 dapat meringankan gejala ini. Selain itu, peningkatan kadar GDF-15 pada pasien kanker dikaitkan dengan penurunan berat badan dan massa otot rangka, penurunan kekuatan, dan pemendekan kelangsungan hidup, yang menggarisbawahi nilai GDF-15 sebagai target terapi potensial.
Ponsegromab (PF-06946860) adalah antibodi monoklonal humanisasi yang sangat selektif yang mampu mengikat GDF-15 yang bersirkulasi, sehingga menghambat interaksinya dengan reseptor GFRAL. Dalam uji coba fase 1b label terbuka skala kecil, 10 pasien dengan kaheksia kanker dan peningkatan kadar GDF-15 yang bersirkulasi diobati dengan ponsegromab dan menunjukkan perbaikan berat badan, nafsu makan, dan aktivitas fisik, sementara kadar GDF-15 serum terhambat dan efek sampingnya rendah. Berdasarkan hal ini, kami melakukan uji klinis Fase 2 untuk mengevaluasi keamanan dan efikasi ponsegromab pada pasien dengan kaheksia kanker dengan peningkatan kadar GDF-15 yang bersirkulasi, dibandingkan dengan plasebo, untuk menguji hipotesis bahwa GDF-15 merupakan patogenesis utama penyakit ini.
Penelitian ini melibatkan pasien dewasa dengan cachexia yang terkait dengan kanker (kanker paru-paru non-sel kecil, kanker pankreas, atau kanker kolorektal) dengan kadar serum GDF-15 minimal 1500 pg/ml, skor status kebugaran Eastern Tumor Consortium (ECOG) ≤3, dan harapan hidup minimal 4 bulan.
Pasien yang terdaftar secara acak ditugaskan untuk menerima 3 dosis ponsegromab 100 mg, 200 mg, atau 400 mg, atau plasebo, secara subkutan setiap 4 minggu dengan rasio 1:1:1. Titik akhir primer adalah perubahan berat badan relatif terhadap nilai dasar pada 12 minggu. Titik akhir sekunder utama adalah perubahan dari nilai dasar pada skor Sub-Skala Anoreksia Kakheksia (FAACT-ACS), sebuah penilaian fungsi terapeutik untuk anoreksia kaheksia. Titik akhir sekunder lainnya termasuk skor catatan harian gejala kaheksia terkait kanker, perubahan dasar dalam aktivitas fisik, dan titik akhir gaya berjalan yang diukur menggunakan perangkat kesehatan digital yang dapat dikenakan. Persyaratan waktu pemakaian minimum ditentukan sebelumnya. Penilaian keamanan mencakup jumlah kejadian buruk selama pengobatan, hasil tes laboratorium, tanda-tanda vital, dan elektrokardiogram. Titik akhir eksplorasi mencakup perubahan dasar pada indeks otot rangka lumbal (luas otot rangka dibagi dengan kuadrat tinggi badan) yang terkait dengan otot rangka sistemik.
Sebanyak 187 pasien secara acak dibagi menjadi 46 pasien untuk menerima ponsegromab 100 mg, 46 pasien untuk 200 mg, dan 50 pasien untuk plasebo. Tujuh puluh empat pasien (40 persen) menderita kanker paru non-sel kecil, 59 pasien (32 persen) menderita kanker pankreas, dan 54 pasien (29 persen) menderita kanker kolorektal.
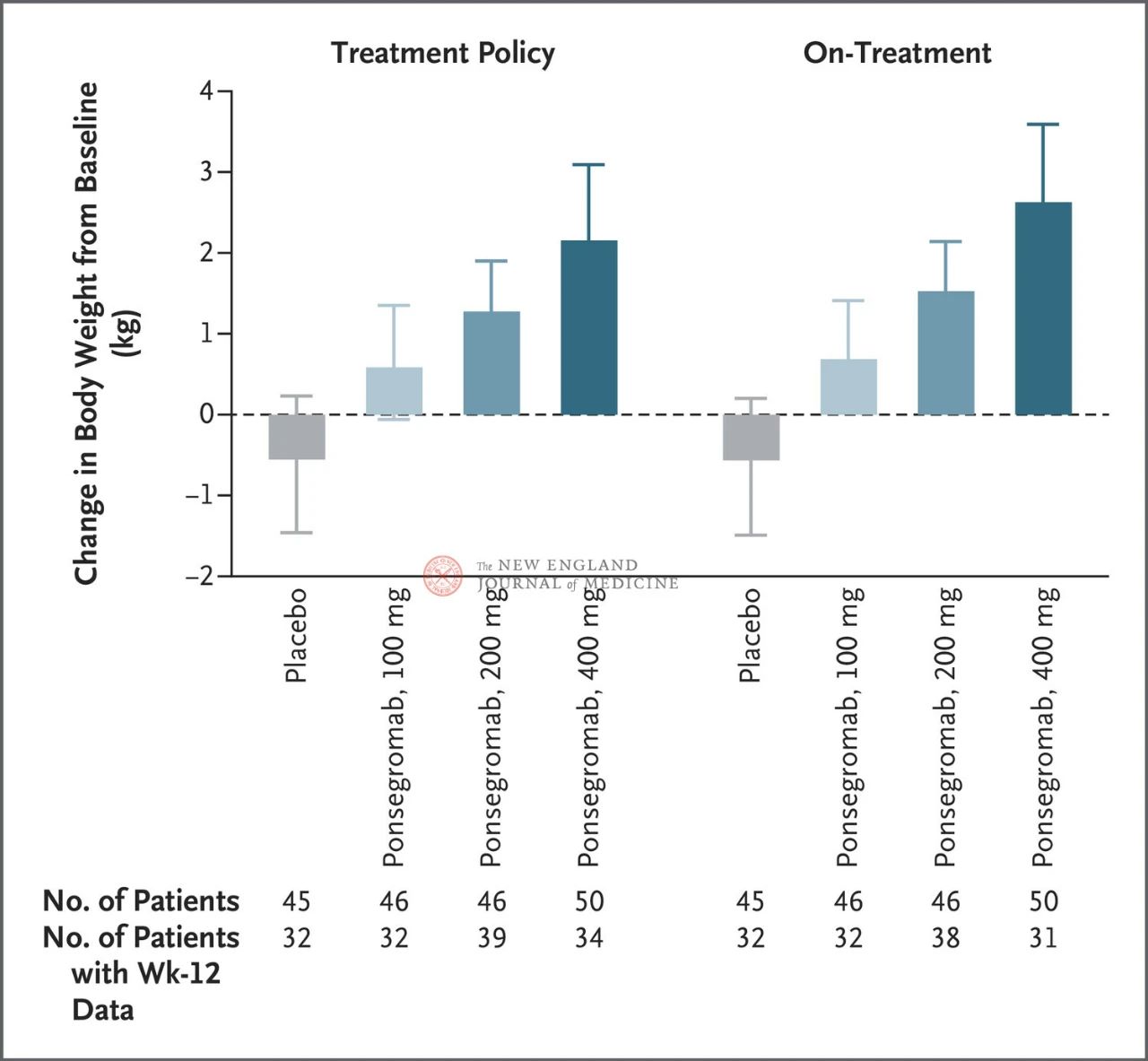
Perbedaan antara kelompok 100 mg, 200 mg, dan 400 mg dan plasebo masing-masing adalah 1,22 kg, 1,92 kg, dan 2,81 kg.
Gambar menunjukkan titik akhir primer (perubahan berat badan dari awal hingga 12 minggu) untuk pasien dengan kaheksia kanker pada kelompok ponsegromab dan plasebo. Setelah disesuaikan dengan risiko kematian dan kejadian bersamaan lainnya, seperti penghentian pengobatan, titik akhir primer dianalisis dengan model Emax terstratifikasi menggunakan hasil minggu ke-12 dari analisis longitudinal gabungan Bayesian (kiri). Titik akhir primer juga dianalisis dengan cara yang serupa, menggunakan target estimasi untuk pengobatan aktual, di mana observasi setelah semua kejadian bersamaan dipotong (gambar kanan). Interval kepercayaan (ditunjukkan dalam artikel)
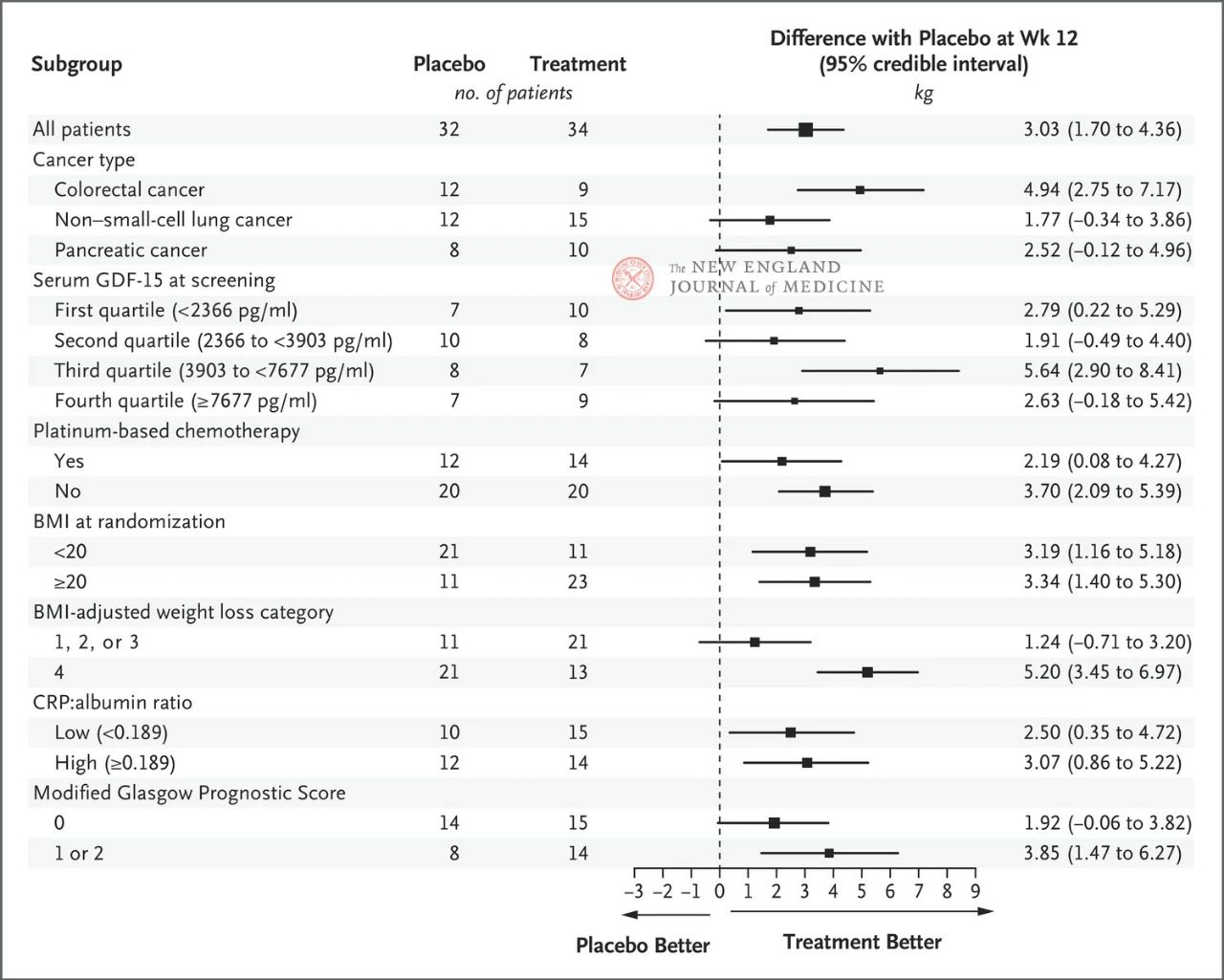
Efek ponsegromab 400 mg terhadap berat badan konsisten di seluruh subkelompok utama yang telah ditentukan sebelumnya, termasuk jenis kanker, kuartil kadar GDF-15 serum, paparan kemoterapi berbasis platinum, IMT, dan peradangan sistemik awal. Perubahan berat badan konsisten dengan penghambatan GDF-15 pada 12 minggu.
Pemilihan subkelompok kunci didasarkan pada analisis longitudinal gabungan Bayesian post-hoc, yang dilakukan setelah penyesuaian risiko kematian kompetitif berdasarkan estimasi target strategi pengobatan. Interval kepercayaan tidak boleh digunakan sebagai pengganti uji hipotesis tanpa beberapa penyesuaian. BMI mewakili indeks massa tubuh, CRP mewakili protein C-reaktif, dan GDF-15 mewakili faktor diferensiasi pertumbuhan 15.
Pada awal penelitian, proporsi pasien yang lebih tinggi dalam kelompok ponsegromab 200 mg tidak melaporkan penurunan nafsu makan; dibandingkan dengan plasebo, pasien dalam kelompok ponsegromab 100 mg dan 400 mg melaporkan peningkatan nafsu makan dari awal penelitian pada 12 minggu, dengan peningkatan skor FAACT-ACS masing-masing sebesar 4,12 dan 4,5077. Tidak terdapat perbedaan signifikan dalam skor FAACT-ACS antara kelompok 200 mg dan kelompok plasebo.
Karena persyaratan waktu pemakaian yang telah ditentukan sebelumnya dan masalah pada perangkat, 59 dan 68 pasien masing-masing memberikan data tentang perubahan aktivitas fisik dan titik akhir gaya berjalan relatif terhadap kondisi awal. Di antara pasien-pasien ini, dibandingkan dengan kelompok plasebo, pasien dalam kelompok 400 mg mengalami peningkatan aktivitas secara keseluruhan pada minggu ke-12, dengan peningkatan 72 menit aktivitas fisik non-sedentary per hari. Selain itu, kelompok 400 mg juga mengalami peningkatan indeks otot rangka lumbal pada minggu ke-12.
Insiden efek samping adalah 70% pada kelompok ponsegromab, dibandingkan dengan 80% pada kelompok plasebo, dan terjadi pada 90% pasien yang menerima terapi antikanker sistemik secara bersamaan. Insiden mual dan muntah lebih rendah pada kelompok ponsegromab.
Waktu posting: 05-Okt-2024